4.免疫チェックポイント分子
がん細胞は免疫系からの攻撃を回避するために、制御性T細胞(Regulatory T cell:Treg)や骨髄由来抑制細胞(Myeloid-derived suppressor cell:MDSC)のほかに、免疫チェックポイント分子による免疫抑制機能も積極的に活用し、免疫逃避しています。ここでは免疫チェックポイント分子について詳しくみていきます。
免疫チェックポイント分子とは1,2
免疫チェックポイント分子は、免疫恒常性を保つために自己に対する免疫応答を抑制するとともに、過剰な免疫反応を抑制する分子群です。本来、T細胞の過剰な活性化を抑制するとともに、自己を攻撃しないために存在していますが、発がん過程では、がん細胞が免疫系からの攻撃を回避し増殖するために利用されます。現在、さまざまな免疫チェックポイント分子とそのリガンドが同定されていますが(下図)3、ここでは特にCTLA-4とPD-1について解説します。
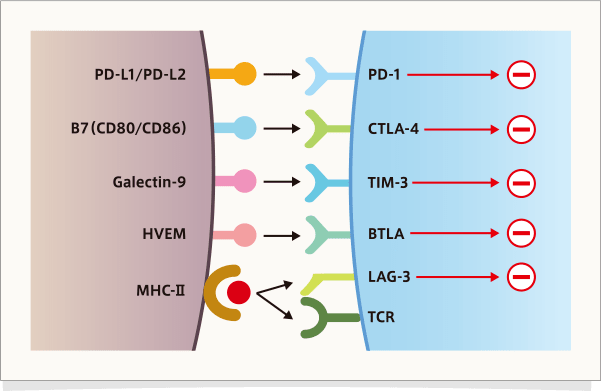
文献3より抜粋、改変
CTLA-4(Cytotoxic T-lymphocyte associated antigen-4)1,4-6
CTLA-4はT細胞を抑制する免疫チェックポイント分子として機能しています。定常状態のT細胞には発現しておらず、T細胞の活性化に伴い発現が誘導されます。また、免疫抑制機能を有するTreg上には恒常的に発現しています。 T細胞は、T細胞受容体(T-cell receptor:TCR)を介したがん抗原認識による抗原(主刺激)シグナルと、共刺激分子であるCD28と抗原提示細胞上のB7(CD80/CD86)の結合による共刺激シグナルによって活性化します(下図A)。しかしCTLA-4は、CD28のリガンドであるB7(CD80/CD86)に対してCD28よりも高い親和性を有するために、T細胞にCTLA-4が多く発現している状態ではB7(CD80/CD86)が占有され、CD28はB7(CD80/CD86)と結合できず、T細胞活性化が抑制されます(下図B)。また、TregはCTLA-4を介してB7(CD80/CD86)の発現を抑制し、抗原提示細胞の成熟を抑制するため、共刺激シグナルが阻害され、T細胞の活性化が抑制されます(下図C)。
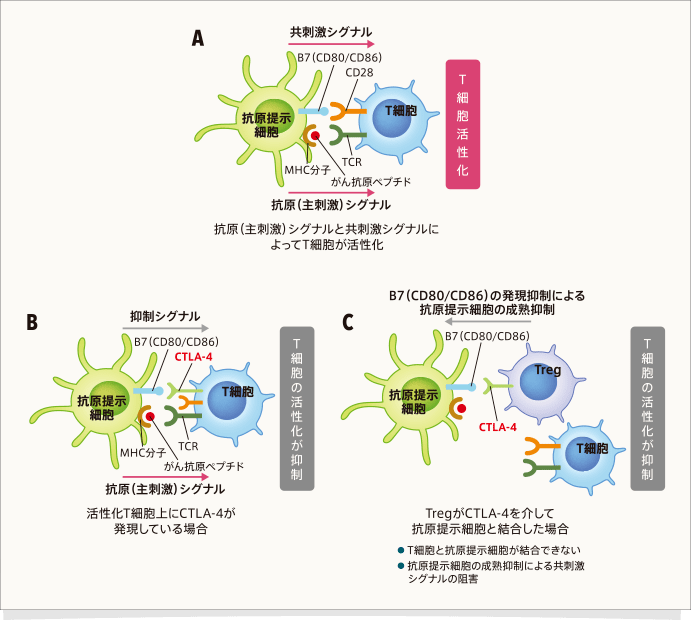
文献1,4-6より作成
PD-1(Programmed-cell death-1/CD279)
PD-1は活性化T細胞に発現する免疫チェックポイント分子であり、代表的なリガンドはPD-L1、PD-L2です1,7。T細胞上のPD-1がPD-L1やPD-L2と結合すると、T細胞は活性化が抑制され機能不全に陥り、抗腫瘍免疫応答が抑制されます1,4。
PD-L1は、抗原提示細胞やがん細胞(肺がん、大腸がん、悪性黒色腫など)で発現がみられます1,7,8。がん細胞自身の遺伝子異常に由来して発現が誘導、上昇している場合と、活性化T細胞が放出する炎症性サイトカインのIFN-γによってがん細胞上に発現が誘導される場合があります7。PD-L2は活性化した抗原提示細胞やマクロファージ7のほか、がん細胞においても発現が認められています9。
がん細胞は、自身に発現したPD-L1/PD-L2を、がん組織に集まってきたT細胞のPD-1と結合させることで免疫逃避していると考えられます7。
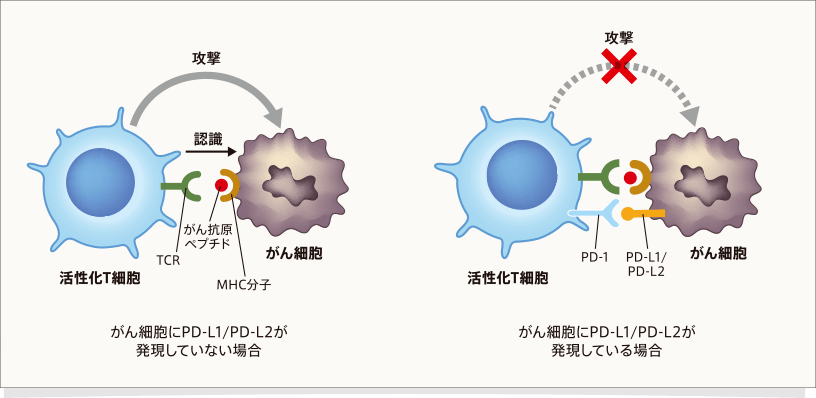
文献1,4より作成
CTLA-4はがん免疫応答のしくみ(Cancer-Immunity Cycle)のなかで、T細胞の活性化(プライミング相、下図STEP③)の部分でがん免疫応答にブレーキをかけています。PD-1やPD-L1/PD-L2は、がん細胞への攻撃(エフェクター相、下図STEP⑦)の部分でがん免疫応答にブレーキをかけているほか、T細胞の活性化(プライミング相、下図STEP③)の部分でも免疫応答を阻害していると考えられます10,11。
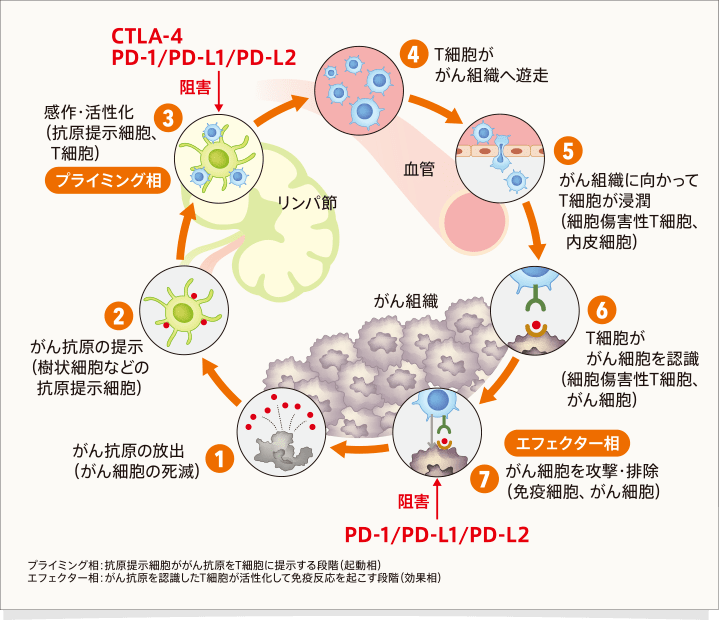
文献11より作成
REFERENCES
- 坂口志文ほか 編. がんと免疫, p120-129, 南山堂, 2015
- 高塚奈津子ほか. 臨床泌尿器科. 2017;71:16-22.
- 玉田耕治. やさしく学べる がん免疫療法のしくみ, p26-38, 羊土社, 2016
- 杉山栄里ほか. Pharma Medica. 2016;34:23-27.
- 竹内美子ほか. 医学のあゆみ. 2016;258:97-105.
- 坂口志文ほか 編. がんと免疫, p97-98, 南山堂, 2015
- 岡三喜男. 読んで見てわかる免疫腫瘍学, p114, 中外医学社, 2017
- 坂口志文ほか 編. がんと免疫, p118, 南山堂, 2015
- Taube JM, et al. Clin Cancer Res. 2014;20:5064-5074.
- Vasaturo A, et al. Front Immunol. 2013;4:417.
- Chen DS, et al. Immunity. 2013;39:1-10.
















