5.免疫チェックポイント阻害薬1,2
がん細胞は、免疫系から逃避し生き延びるために、免疫チェックポイント分子による免疫抑制機能を活用しています(詳細は 4.
免疫チェックポイント分子を参照)。免疫チェックポイント阻害薬は、免疫チェックポイント分子もしくはそのリガンドに結合して免疫抑制シグナルの伝達を阻害することで、免疫チェックポイント分子によるT細胞の活性化抑制を解除します。
現在、臨床応用が進んでいる主な免疫チェックポイント阻害薬には、抗CTLA-4抗体、抗PD-1抗体、抗PD-L1抗体などがあります。
抗CTLA-4抗体1,3,4,5
CTLA-4は、活性化T細胞や制御性T細胞(Regulatory T
cell:Treg)上に発現し、抗原提示細胞上のB7(CD80/CD86)と結合することで、T細胞の活性化を抑制します1,3,4(下図A)(詳細は 4.
免疫チェックポイント分子を参照)。
抗CTLA-4抗体は、CTLA-4とB7(CD80/CD86)との結合を阻害することで、T細胞上の共刺激分子であるCD28とB7(CD80/CD86)の結合を可能にし、T細胞を再活性化します1,3,4,5(下図B)。また、Treg上のCTLA-4に結合し、Tregの免疫抑制機能を低下させるとともに、ADCC(Antibody-dependent-cellular-cytotoxicity:抗体依存性細胞傷害)により腫瘍組織中のTregを減少させることで抗原提示細胞を成熟させてT細胞を活性化し、T細胞が抗腫瘍効果を発揮することを促進します1,4,5。
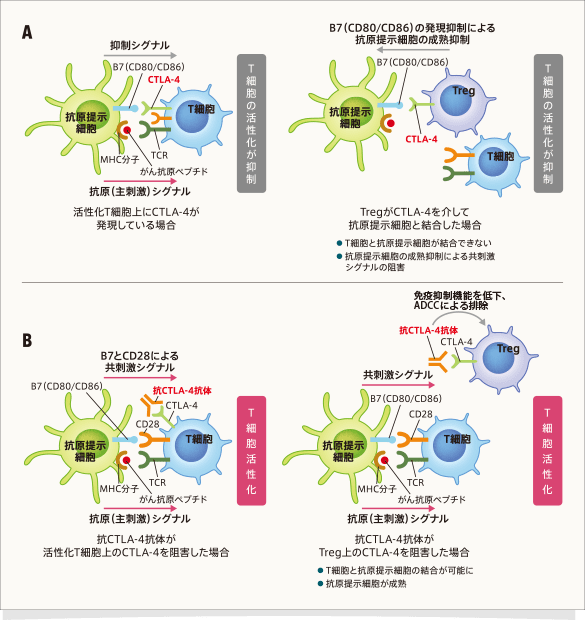
文献1,3,4,5より作成
抗PD-1抗体、抗PD-L1抗体
活性化T細胞上に発現しているPD-1が、がん細胞や抗原提示細胞に発現したPD-L1やPD-L2と結合すると、T細胞活性化は抑制され、がん細胞の免疫逃避を引き起こします3(詳細は 4.
免疫チェックポイント分子を参照)。
抗PD-1抗体は、T細胞上のPD-1に結合してPD-1とPD-L1/PD-L2の結合を阻害することにより、抑制シグナルの伝達をブロックしてT細胞の活性化を維持し、抗腫瘍効果を回復させます6。
抗PD-L1抗体※は、がん細胞や抗原提示細胞が発現するPD-L1に結合することによりT細胞上のPD-1との相互作用を阻害します。その結果T細胞への抑制シグナル伝達が阻害され、T細胞の活性化が維持されます4,
6。
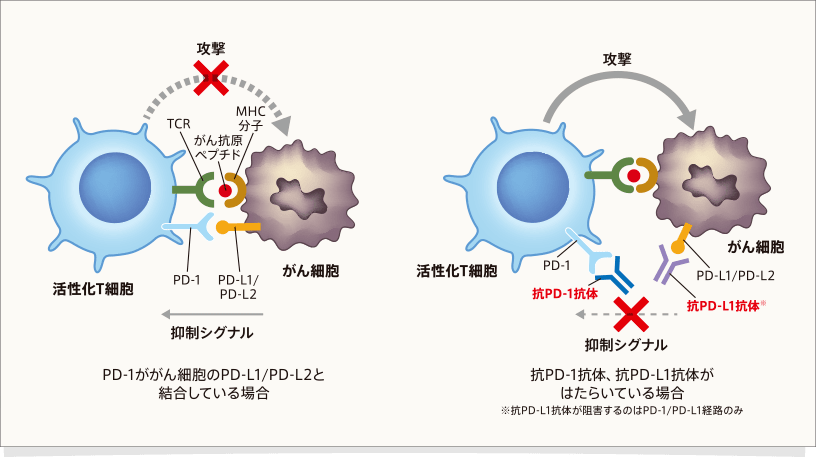
文献3,4,6より作成
抗CTLA-4抗体は、がん免疫応答のしくみ(Cancer-Immunity
Cycle)のなかの、T細胞の活性化(プライミング相、下図STEP③)の部分で、CTLA-4によるがん免疫応答のブレーキを解除します。抗PD-1抗体/抗PD-L1抗体は、がん細胞への攻撃(エフェクター相、下図STEP⑦)の部分で、PD-1とPD-L1/PD-L2※によるがん免疫応答のブレーキを解除するほか、T細胞の活性化(プライミング相、下図STEP③)の部分でも免疫応答の阻害を解除すると考えられています7,8。
※PD-1/PD-L2経路の阻害は抗PD-1抗体のみ
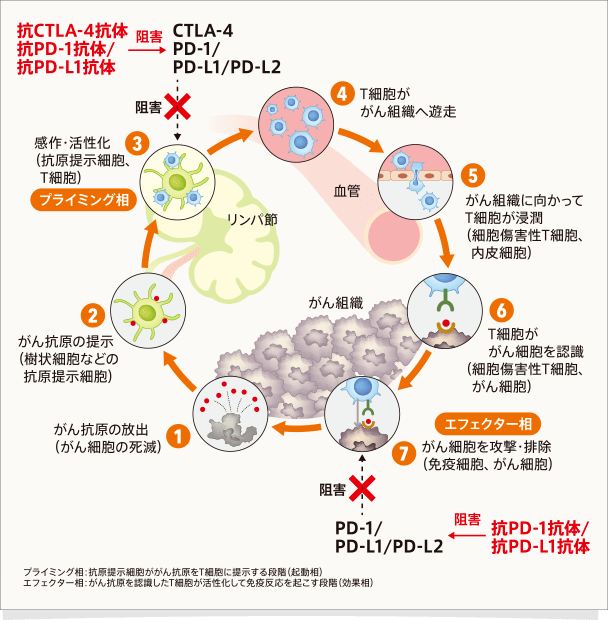
文献8より作成
REFERENCES
- 杉山栄里ほか. Pharma Medica. 2016;34:23-27.
- 竹内美子ほか. 医学のあゆみ. 2016;258:97-105.
- 坂口志文ほか 編. がんと免疫, p120-129, 南山堂, 2015
- Malas S, et al. Oncol Rep. 2014;32:875-886.
- 天野学ほか. 日本薬理学雑誌 147(4):243-252, 2016
- 上田龍三 監, 西川博嘉 編. がん免疫療法ハンドブック, p48-50, メディカルレビュー社, 2016
- Vasaturo A, et al. Front Immunol. 2013;4:417.
- Chen DS, et al. Immunity. 2013;39:1-10.
















